Temperaturmapping von heute: Was sich geändert hat, was nicht und was am wichtigsten ist

In der Welt der regulierten Fertigung ist das Temperaturmapping seit Langem ein grundlegendes Validierungstool – entscheidend zur Gewährleistung der Sicherheit und Wirksamkeit von Arzneimitteln, Biologika und Medizinprodukten. Für diejenigen, die Lager, Labors, Kühlschränke, Gefrierschränke oder Reinräume in GxP-regulierten Umgebungen verwalten, ist es wichtig, die tiefere Rolle des Mappings zu verstehen – nicht nur als Kontrollkästchenaktivität, sondern als Validierung selbst.
Mapping ist mehr als nur Überwachung
Moderne Überwachungssysteme bieten Daten in Echtzeit, automatisierte Alarme und auditfähige Aufzeichnungen. Es wird angenommen, dass dies ausreicht. Allerdings erfüllen Überwachung und Mapping ganz unterschiedliche Aufgaben. Während die Überwachung sicherstellt, dass ein bekanntes System innerhalb der Spezifikationen bleibt, beweist das Mapping, dass das System in der Lage ist, diese Spezifikationen einzuhalten – an allen Stellen und unter realen Bedingungen. Mapping ist Validierung. Es qualifiziert ein temperaturgeregeltes Gerät (CTU) oder einen Bereich, indem es die Einheitlichkeit und Eignung für die Lagerung empfindlicher oder hochwertiger Produkte nachweist.

Warum Mapping?
Wenn Sie bislang keine Mappingstudie zu Ihrer GxP-regulierten Anwendung durchgeführt haben, setzen Sie im Wesentlichen Ihr Produkt aufs Spiel. Dennoch erreicht uns von Kunden immer wieder folgende Frage:
„Muss ich ein Mapping durchführen, wenn ich mit zuverlässigen, kalibrierten Sensoren überwache?“
Die kurze Antwort lautet: Ja, das müssen Sie.
Zwar gibt es sicherlich Anlagen, die direkt mit der Überwachung beginnen und die Mappingphase überspringen, aber das macht den Ansatz weder konform noch sinnvoll. Vorschriften, einschließlich derjenigen der FDA- und EU-GMP-Anhänge, erfordern eindeutig ein Temperaturmapping als Voraussetzung für die Umgebungsüberwachung. Und das aus gutem Grund.
Durch das Mapping wird das Umgebungsprofil eines Bereichs erstellt. Es identifiziert, wie sich Temperatur (und andere Parameter wie Feuchte oder Differenzdruck) im Laufe der Zeit und an verschiedenen Stellen innerhalb eines kontrollierten Bereichs verhält. Ohne diese Daten fischen Sie eigentlich im Trüben. Sie würden nicht wissen, wo die wärmsten oder kältesten Stellen sind – oder wie sich äußere Bedingungen auf die innere Stabilität auswirken.
Während einige Branchenfachleute die Vorstellung von „heißen Stellen“ und „kalten Stellen“ herunterspielen, bleibt die Tatsache bestehen: Ohne Mapping weiß man nie, ob und wo sie existieren. Durch das Mapping werden die erforderlichen Nachweise geliefert, um Überwachungssensoren intelligent zu platzieren – dort, wo sie am wahrscheinlichsten aussagekräftige Daten erfassen.
Was ist, wenn ich (wirklich, ehrlich) kein Mapping durchführen kann?
Es stimmt, dass, wenn Sie gezwungen wären, nur eine Option zu wählen, die Überwachung den Nachweis liefern würde, dass mindestens eine Stelle in Ihrem Bereich den Spezifikationen entsprach. Aber das ist eine falsche Wahl. Mapping und Überwachung dienen unterschiedlichen, aber sich ergänzenden Zwecken. Das Überspringen des Mappings ist nicht nur eine Abkürzung – es beeinträchtigt auch die Konformität und gefährdet die Produktqualität.
Insbesondere in Umgebungen der guten Vertriebspraxis (GDP) ist das Mapping ein Bereich, der mehr Aufmerksamkeit verdient. Durch frühzeitige Investitionen in ein ordnungsgemäßes Mapping wird auf lange Sicht die Überwachung intelligenter gestaltet und die Konformität verbessert. Sehen wir uns genauer an, warum Mappingstudien immer noch wichtig sind.
Mapping in einer Welt nach Einführung von GDP
Die Einführung der guten Vertriebspraxis (GDP) brachte einen grundlegenden Wandel mit sich. Während das Temperaturmapping früher als bewährte Methode galt, ist es heute in den Vorschriften für Lager und Vertrieb festgeschrieben. Diese Ausweitung der Verantwortung fällt jedoch häufig den Anlagen zu, die über begrenzte Budgets und weniger ausgereifte Qualitätsmanagementsysteme (QMS) verfügen. Diesen Umgebungen fehlt das prozedurale Rückgrat, das echte Validierung ermöglicht. Beim Mapping ohne ein fundiertes QMS besteht die Gefahr, dass Daten mit eingeschränkter Aussagekraft – oder schlimmer noch, irreführend – erstellt werden.
In solchen Fällen kann die Implementierung eines validierten Überwachungssystems eine gleichbleibendere Qualitätssteuerung bieten als eine schlecht ausgeführte Mappingstudie. Dennoch bleibt das Mapping für zentrale GMP-Anlagen unersetzlich. Es stellt sicher, dass jeder Kubikmeter Ihrer Umgebung die Lagerspezifikationen erfüllt, die Sie Ihren Aufsichtsbehörden und Ihren Patienten versprechen.
Geräte und Datenintegrität
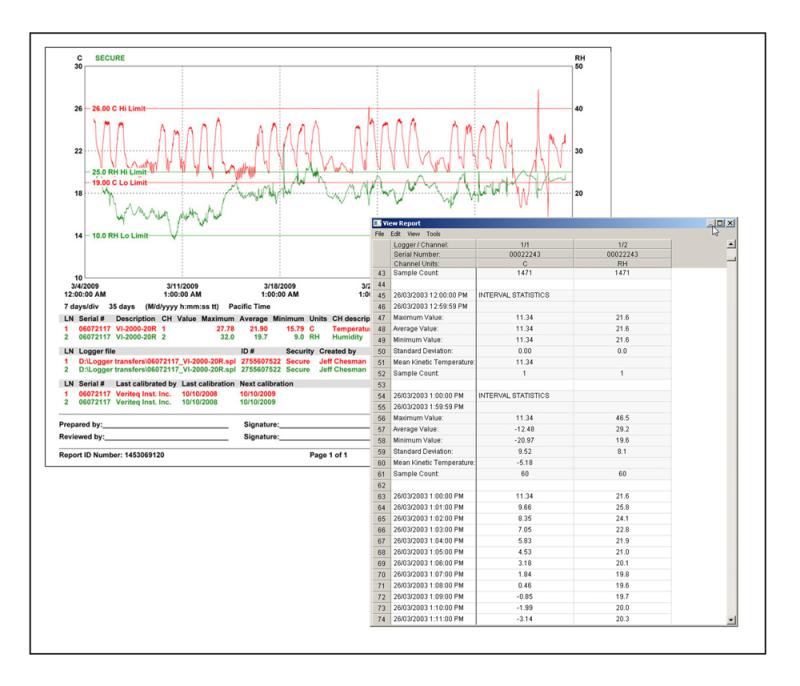
Die häufigste Stolperfalle beim Temperaturmapping besteht darin, an Geräten zu sparen. Kostengünstige Logger sparen zwar zunächst Geld, gefährden aber die Studienergebnisse. Die Mappinggenauigkeit basiert auf hochwertigen, gut kalibrierten Sensoren – aufgrund ihrer Stabilität vorzugsweise Widerstandsthermometer gegenüber Thermoelementen. Sie möchten außerdem Datenprotokollierungssoftware mit ausreichend Speicher und Software, die die Analyse und Berichterstellung optimiert. Aus regulatorischer Sicht bewertet das Prüfpersonal Ihr Qualitätsmanagement mithilfe der Mappingdaten. Die Kalibrierung konnte nicht verifiziert werden? Sie werden nach Ihren Standardarbeitsanweisungen gefragt. Es fehlt eine Unterschrift? Es wird Ihre Dokumentenkontrolle in Frage gestellt. Fehler bei Mappingaufzeichnungen führen häufig zu einer genaueren Prüfung.
Erneutes Mapping neu durchdacht: Von der Routine zu risikobasiert
Ein weiterer Bereich, der sich weiterentwickelt, ist die Häufigkeit von erneutem Mapping. Viele Organisationen führen in festgelegten Abständen – jedes Jahr oder alle drei Jahre – ein erneutes Mapping durch, ohne zu überprüfen, ob dies wirklich notwendig ist. Ein strategischerer Ansatz, der durch die jüngsten Aktualisierungen der Leitlinien gefördert wird, besteht darin, Risikobewertungen einzusetzen, um festzustellen, wann ein erneutes Mapping gerechtfertigt ist. Dadurch wird unnötiger Aufwand vermieden und sichergestellt, dass Ihre Ressourcen dort genutzt werden, wo sie die größte Wirkung erzielen.
Internes Mapping oder ausgelagertes Mapping
Müssen Sie Ihr eigenes Mappingprogramm erstellen oder auslagern? Die Entscheidung hängt von zwei wichtigen Faktoren ab: Häufigkeit und Vertrautheit. Wenn Sie regelmäßig Temperaturmapping durchführen und über die entsprechenden Tools und Fachkenntnisse verfügen, kann internes Mapping effizient sein. Wenn Sie sich jedoch nicht sicher sind, wie Sie Sensoren wählen, Protokolle entwerfen oder Ergebnisse interpretieren, ist die Beauftragung eines qualifizierten Serviceanbieters häufig die intelligentere (und sicherere) Entscheidung. Beobachten Sie die Fachleute ein paar Mal dabei und entwickeln Sie die Fähigkeiten, die Sie brauchen, um es schließlich intern umzusetzen.

Wegweisende Technologie
Moderne Innovationen – wie drahtlose Datenlogger mit sicherer Übertragung mit hoher Reichweite – gestalten das Lagermapping einfacher und sicherer. Diese Tools ermöglichen Dateneinblicke in Echtzeit während der Qualifizierung, sodass die Teams Probleme erkennen und Anpassungen vornehmen können, bevor sie die Arbeit investieren, um Logger aus etwa 9 Metern Höhe zu bergen. Durch weniger Wiederholungsprüfungen und weniger Ausfallzeiten senkt diese Technologie die Kosten, verbessert die Ergebnisse und verhindert Überraschungen bei Audits.
Abschließender Rat: Verfahren umsetzen, mit Abweichungen rechnen
Bei jedem Mappingprojekt, bei dem viel auf dem Spiel steht oder bei dem es sich um ein erstes Projekt handelt, ist ein Ratschlag wichtiger als alle anderen: Seien Sie geduldig. Mapping und Validierung brauchen Zeit und der Versuch, sie zu überstürzen, führt garantiert zu Stress, Fehlern oder schlimmer noch, Nichtkonformität.
Akzeptieren Sie, dass Abweichungen auftreten werden. Tatsächlich verraten sie oft mehr über das Verfahren als eine perfekte Ausführung. Eine gut dokumentierte Abweichung zeigt, dass Sie Ihr System verstehen. Eine makellose Ausführung hingegen kann Fragen aufwerfen, ob es wirklich so perfekt ist.
Schlussfolgerung
Temperaturmapping ist gesetzlich vorgeschrieben und unabhängig davon, ob Sie einen einzelnen Blutbankkühlschrank oder ein ganzes Biologikalager verwalten, geht es bei einer durchdachten Mappingstrategie – unterstützt durch die geeigneten Tools, Arbeitskräfte und Prozesse – nicht nur um Konformität. Es ist eine Verpflichtung zur Sicherheit der Patienten, die die Produkte letztendlich verwenden.
Ressourcen

Kontinuierliches Überwachungssystem viewLinc

vLog Mapping-/Validierungssystem

Support und Services
Wir bieten verschiedenste Services zur Unterstützung aller Aspekte Ihres Umgebungsüberwachungssystems – einschließlich Software, Sensoren und Netzwerkkonnektivitätskomponenten. Von der Bereitstellung durch Fachkräfte bis hin zur Schulung statten unsere Services zum kontinuierlichen Überwachungssystem (CMS) Ihr Team mit dem Wissen und den Tools aus, die es braucht, um sicher und konform zu arbeiten. Unabhängig davon, ob Sie ein neues System installieren oder ein vorhandenes optimieren, stellen unsere Services sicher, dass Ihre Überwachungslösung effizient und zuverlässig ist und vollständig den strengsten GxP- und regulatorischen Anforderungen entspricht.
