Comment mesurer le dioxyde de carbone (CO₂)

La mesure du dioxyde de carbone est exigée dans de nombreuses applications, du contrôle automatique des bâtiments aux serres, en passant par les sciences de la vie et la sécurité.
Cet article aborde les sujets suivants :
Principe de fonctionnement des capteurs à infrarouge
Le dioxyde de carbone et d'autres gaz composés d'au moins deux atomes différents absorbent le rayonnement infrarouge (RI) de manière spécifique et unique. Ces gaz sont détectables à l'aide de techniques par RI. La vapeur d'eau, le méthane, le dioxyde de carbone et le monoxyde de carbone sont des exemples de gaz mesurables au moyen d'un capteur à RI. Leurs bandes d'absorption typiques sont présentées dans la figure 1.
la plus utilisée pour la détection du CO2. Comparés aux capteurs chimiques, les capteurs à RI présentent plusieurs avantages. Ils sont stables et hautement sélectifs par rapport au gaz mesuré. Ils ont une durée de vie supérieure et, puisque le gaz mesuré n'interagit pas directement avec le capteur, les capteurs à RI peuvent supporter des niveaux élevés d'humidité, de poussière, d'encrassement et d'autres conditions exigeantes.
Les principaux composants d'un détecteur à RI de CO2 sont la source lumineuse, la chambre de mesure, le filtre interférentiel et le détecteur de RI. Le rayonnement IR part de la source lumineuse, traverse le gaz mesuré pour atteindre le détecteur. Un filtre placé à l'avant du détecteur empêche les ondes différentes de celles spécifiées pour le gaz mesuré, d'accéder au détecteur. L'intensité lumineuse est détectée et convertie en une valeur de concentration du gaz.
Le capteur de dioxyde de carbone CARBOCAP® de Vaisala utilise une technologie de détection par RI pour mesurer la concentration volumique du CO2. Il comprend un interféromètre Fabry-Perot (IFP) électrique accordable pour la mesure des longueurs d'onde. Cela signifie qu'en plus de mesurer l'absorption du CO2, le capteur CARBOCAP® effectue également une mesure de référence qui compense tous les changements de l'intensité de la source lumineuse, ainsi que l'accumulation de saleté et la contamination. Cela rend le capteur extrêmement sensible et stable. Consultez la gamme complète des produits de Vaisala pour la mesure du CO2 sur le site www.vaisala.com/CO2

Figure 1. Absorption par RI du CO2 et d'autres gaz.
Loi des gaz parfaits
La loi des gaz parfaits permet d'évaluer l'effet des changements de température et de pression sur la mesure du CO2. Elle peut être utilisée pour compenser les lectures de CO2.
Les gaz parfaits sont des gaz fictifs composés de particules identiques qui se déplacent de manière aléatoire, sont de taille négligeable et possèdent des forces intermoléculaires également négligeables. Les molécules des gaz parfaits sont supposées subir des collisions élastiques aussi bien les unes avec les autres qu'avec les parois du conteneur.
En réalité, les gaz ne se comportent pas exactement comme les gaz parfaits, mais cette approximation est le plus souvent utilisée pour décrire le comportement des gaz réels. La loi des gaz parfaits permet d'évaluer la relation entre l'état d'une certaine quantité de gaz et sa pression, son volume et sa température, en fonction de l'équation :
pV = nRT
où :
p = pression [Pa]
V = volume du gaz [m3]
n = quantité de gaz [mol]
R = constante universelle du gaz (= 8.3145 J/mol K)
T = température [K]

Figure 2. La structure du capteur de CO2 CARBOCAP® Vaisala.
Augmentation de la pression à température constante
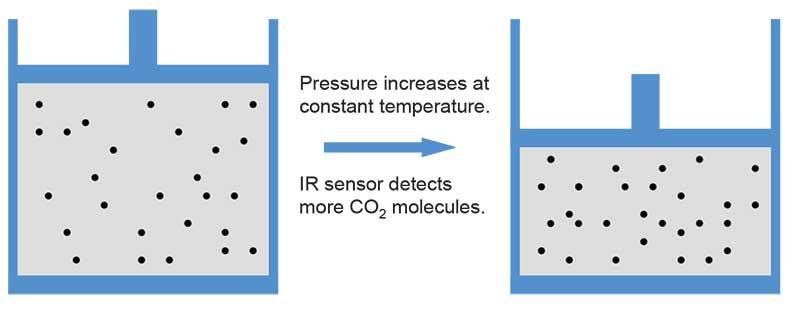
Augmentation de la température à pression constante

Emplacements optimaux des transmetteurs de CO₂
- Évitez les emplacements où des gens peuvent respirer directement sur le capteur. Évitez également de placer les capteurs à proximité des conduits d'aération ou d'évacuation, près des fenêtres ou des portes.
- Pour la ventilation contrôlée à la demande, les capteurs muraux fournissent des données plus précises sur l'efficacité de la ventilation que les capteurs sur gaine. Les capteurs sur gaine sont adaptés aux systèmes à zone unique et doivent être installés le plus près possible de l’espace occupé, avec un accès dégagé pour la maintenance.
- Lorsque vous mesurez le CO2 pour assurer la sécurité du personnel, les transmetteurs doivent être installés près des points de fuite potentielle afin de permettre une détection rapide. La géométrie, la ventilation et le débit d'air de la zone surveillée doivent être pris en compte. Le nombre et l'emplacement des transmetteurs de CO2 doivent résulter d'une évaluation du risque.
L'effet de la température et de la pression sur la mesure du CO₂
La majorité des capteurs de gaz émettent un signal proportionnel à la densité moléculaire (molécules/ volume du gaz), même si la lecture est exprimée en parties par million (volume/volume). Selon la loi des gaz parfaits, la pression et/ou la température change au fur et à mesure que la densité moléculaire du gaz évolue. L'effet est perçu dans la lecture ppm du capteur.
Les illustrations suivantes montrent comment une augmentation de la pression ou de la température modifie l'état du gaz et comment elle influence la mesure du CO2.
calculer la densité moléculaire d'un gaz à une température et une pression données, lorsque la densité du gaz à une température et une pression ambiantes standard (CNTP) est connue. En remplaçant la quantité de gaz (n) par ρV/M, et en supposant que la masse molaire du gaz (M) est constante dans les deux différentes conditions, l'équation peut être écrite comme suit dans l'équation 1.

où :
ρ = concentration du volume de gaz [ppm ou %]
p = pression ambiante [hPa]
t = température ambiante [°C]
Équation 1. Calcul de la concentration de gaz à une température et une pression donnée.
La formule de la densité peut servir à estimer comment la lecture du capteur de gaz change proportionnellement à la variation de température et/ou de pression.
La formule de la densité peut servir à compenser les variations de température et de pression au moment de mesurer le CO2. La plupart des instruments de mesure du CO2 ne mesurent pas la pression et, par conséquent, ne peuvent pas automatiquement compenser les variations de pression. Lors de l'étalonnage en usine, les instruments sont typiquement réglés pour les conditions de pression au niveau de la mer (1 013 hPa). En effectuant des mesures à des altitudes autres que celles du niveau de la mer, il est recommandé de compenser l'effet de la pression. Pour ce faire, il faut soit entrer les paramètres de pression exacts pour la compensation interne (conditions de pression constante), soit programmer la compensation dans un système d'automatisation ou un PC (modification des conditions de pression).
Les mêmes règles de compensation s'appliquent à l'effet de la température. Toutefois, il existe de plus en plus de capteurs de CO2 disponibles, qui exécutent à la fois les fonctions de mesure et de compensation des variations de température. Par conséquent, ils ne nécessitent aucune compensation externe.
Le tableau 1 présente un exemple des changements de lecture du capteur de CO2 (le gaz contient 1 000 ppm de CO2 au CNTP) au fur et à mesure que la température et la pression varient, selon la loi des gaz parfaits.
| Température (°C) | ||||||||||
| Pression (hPa) | -20 | -10 | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 |
| 700 | 814 | 783 | 754 | 728 | 703 | 691 | 680 | 658 | 638 | 618 |
| 800 | 930 | 895 | 862 | 832 | 803 | 790 | 777 | 752 | 729 | 707 |
| 900 | 1046 | 1007 | 970 | 936 | 904 | 888 | 874 | 846 | 820 | 795 |
| 1000 | 1163 | 1119 | 1078 | 1039 | 1004 | 987 | 971 | 940 | 911 | 883 |
| 1013 | 1178 | 1133 | 1092 | 1053 | 1017 | 1000 | 983 | 952 | 923 | 895 |
| 1100 | 1279 | 1230 | 1185 | 1143 | 1104 | 1086 | 1068 | 1034 | 1002 | 972 |
| 1200 | 1395 | 1342 | 1293 | 1247 | 1205 | 1185 | 1165 | 1128 | 1093 | 1060 |
| 1300 | 1512 | 1454 | 1401 | 1351 | 1305 | 1283 | 1262 | 1222 | 1184 | 1148 |
Tableau 1. Lecture en ppm du capteur de CO2 lors de la mesure d'un gaz à une concentration de 1 000 ppm
sous différentes conditions de température et de pression.
Séchage d'un échantillon de gaz humide
La loi des gaz parfaits permet également de comprendre ce qui se produit lorsque la composition d'un mélange gazeux varie à pression, température et volume constants. Ceci peut servir, par exemple, à estimer l'effet de la variation de l'humidité sur la lecture du CO2.
Les molécules d'un mélange gazeux sont présentes dans le même volume du système (V est le même pour tous les gaz) à la même température. La loi des gaz parfaits peut être modifiée en :

où :
ngas1 =quantité de gaz 1 [mol]
ngas2 = quantité de gaz 2 [mol], etc.
et

où :
p = pression totale du mélange gazeux
pgas1 = pression partielle du gaz 1
pgas2 = pression partielle du gaz 2, etc.
La deuxième équation est appelée Loi des pressions partielles de Dalton. Elle stipule que dans tout mélange de gaz, la pression totale des gaz est égale à la somme des pressions partielles des gaz constitutifs du mélange.
Cette information est utile pour prendre en compte l'influence de la vapeur d'eau sur l'indication d'un capteur de CO2. Lorsque la vapeur d'eau est ajoutée à un gaz sec à pression, température et volume constants, l'eau remplace certaines molécules de gaz dans le mélange. De même, lorsqu'un échantillon de gaz est tiré d'un environnement à forte humidité, et est séché avant d'être introduit dans la chambre de mesure d'un capteur de CO2, la perte de molécules d'eau change la composition du gaz et a un effet sur la mesure du CO2.
Cet effet, communément appelé effet de dilution peut être estimé à l'aide du tableau 2. La concentration de CO2 dans un environnement à forte humidité peut être calculée lorsque la concentration de CO2 du gaz sec est connue. Pour ce faire, le point de rosée (Td à 1 013 hPa) ou la concentration de l'eau (ppm) dans les conditions sèches et humides doivent être connu(e). La condition de l'humidité de l'environnement à forte humidité est choisie à partir de l'axe horizontal et la condition du gaz sec à partir de l'axe vertical.
Exemple : Un échantillon de gaz est déplacé d'un environnement dont le point de rosée est de 40 °C (73 000 ppm d'eau) à un environnement de 20 °C Td (23 200 ppm d'eau). La concentration de CO2, égale à 5,263 %, mesurée à 20 °C Td passe à 5,00 % dans un environnement à 40 °C Td (5,263 % × 0,950 = 5,00 %). La lecture inférieure résulte de la dilution provoquée par la quantité d'eau plus élevée à 40 °C Td
| Td(°C) | -40 | -30 | -20 | -10 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| Td(°C) | ppm H2O | 127 | 377 | 1 020 | 2 580 | 6 060 | 12 200 | 23 200 | 42 000 | 73 000 | 122 000 | 197 000 |
| -60 | 11 | 0.9999 | 0.9996 | 0.999 | 0.997 | 0.994 | 0.988 | 0.977 | 0.958 | 0.927 | 0.878 | 0.803 |
| -50 | 39 | 0.9999 | 0.9997 | 0.999 | 0.997 | 0.994 | 0.988 | 0.977 | 0.958 | 0.927 | 0.878 | 0.803 |
| -40 | 127 | 1.0000 | 0.9997 | 0.999 | 0.998 | 0.994 | 0.988 | 0.977 | 0.958 | 0.927 | 0.878 | 0.803 |
| -30 | 377 | 1.0000 | 0.999 | 0.998 | 0.994 | 0.988 | 0.977 | 0.958 | 0.927 | 0.878 | 0.803 | |
| -20 | 1 020 | 1.000 | 0.998 | 0.995 | 0.989 | 0.978 | 0.959 | 0.928 | 0.879 | 0.804 | ||
| -10 | 2 580 | 1.000 | 0.997 | 0.990 | 0.979 | 0.961 | 0.930 | 0.880 | 0.805 | |||
| 0 | 6 050 | 1.000 | 0.994 | 0.983 | 0.964 | 0.933 | 0.884 | 0.809 | ||||
| 10 | 12 200 | 1.000 | 0.989 | 0.970 | 0.939 | 0.890 | 0.815 | |||||
| 20 | 23 200 | 1.000 | 0.981 | 0.950 | 0.901 | 0.826 | ||||||
| 30 | 42 000 | 1.000 | 0.969 | 0.920 | 0.845 | |||||||
| 40 | 73 000 | 1.000 | 0.951 | 0.876 | ||||||||
| 50 | 122 000 | 1.000 | 0.925 | |||||||||
| 60 | 197 000 | 1.000 |
Tableau 2. Coefficients de dilution lors du séchage de l'échantillon de gaz.
Dioxyde de carbone et sécurité
Effet des différents niveaux de CO2 | |
| CONCENTRATION | EFFET |
| 350 - 450 ppm | Concentration atmosphérique typique |
| 600 - 800 ppm | Qualité acceptable de l'air intérieur |
| 1,000 ppm | Qualité tolérable de l'air intérieur |
| 5,000 ppm | Limite moyenne d'exposition d'au plus 8 heures |
| 6,000 - 30,000 ppm | Danger, courte exposition uniquement |
| 3 - 8% | Augmentation de la fréquence respiratoire, maux de tête |
| > 10% | Nausée, vomissement, perte de conscience |
| > 20% | Perte rapide de conscience, mort |
Le dioxyde de carbone est un gaz non-toxique et ininflammable. Toutefois, l'exposition à de grandes concentrations peut présenter un danger. À chaque utilisation, production, expédition ou stockage du CO2 ou de la glace sèche, la concentration de CO2 peut augmenter au point d'atteindre des niveaux dangereux. La nature inodore et incolore du CO2 le rend indétectable. C'est pourquoi l'utilisation de capteurs appropriés est nécessaire pour assurer la sécurité du personnel.